1、四川首次成功创制6种基因编辑猪!
记者4日从四川省科技厅获悉,四川农业大学牵头承担的“十四五”主要畜禽分子育种平台项目在川猪领域取得突破性成效,在国内外首次成功创制了6种基因编辑猪。

基因编辑猪和正常基因型猪对比。四川省科技厅供图在基因编辑猪的制备方面,四川农业大学首次成功创制猪经济性状改良的6种基因编辑猪,包括骨骼肌生长(FST和ZEBD6基因)、脂肪沉积(PTRF基因)、代谢能力(ASGR1和FAH基因)、“红肉”食用安全性(GTKO基因),开创了对川猪进行有目标的分子设计育种、改造乃至猪经济性状(生长速度、瘦肉率等)精准定向改良的先河,多篇引领性成果发表在《自然-通讯》等国际权威期刊。
四川农业大学还与中国农业大学开展联合科技攻关,首次成功建立当前世界家畜干细胞传代次数最多(260次以上)、可进行多次基因编辑操作的猪原肠化前上胚层多能干细胞(pgEpiSCs)。鉴定75个在pgEpiSCs中具有重要功能的转录因子,采用基因编辑、核移植技术,成功获得源于pgEpiSCs的基因编辑克隆猪。该干细胞系可多基因编辑,周期短、效率高、耐受性好,极大缩短获得多基因编辑克隆猪的时间和成本。
在分子育种技术体系方面,四川农业大学 运用基因组重测序技术鉴定了四川藏猪与西方瘦肉型猪种巴克夏猪高精度基因组变异。运用高通量染色质空间构象捕获技术(Hi-C),重构了猪骨骼肌、脂肪高分辨率染色质空间构象图谱。发掘了四川藏猪优良肉质相关的关键特色基因DITT4L、KCNC4、CTSB和TUT7及促进骨密度基因PHOSPHO1。
在肌纤维生长与功能基因解析方面,四川农业大学采用空间转录组技术,首次从单肌纤维水平揭示了猪肉质性状形成的基因表达调控分子机理,挖掘其能量代谢、肌纤维组成及脂质沉积的分子调控差异,筛选肌纤维类型决定的候选基因446个。构建了猪全身47种不同解剖学部位骨骼肌精细基因转录调控图谱。(来源:中新网 记者:贺劭清)
2、研究建立高效制备基因编辑猪技术体系
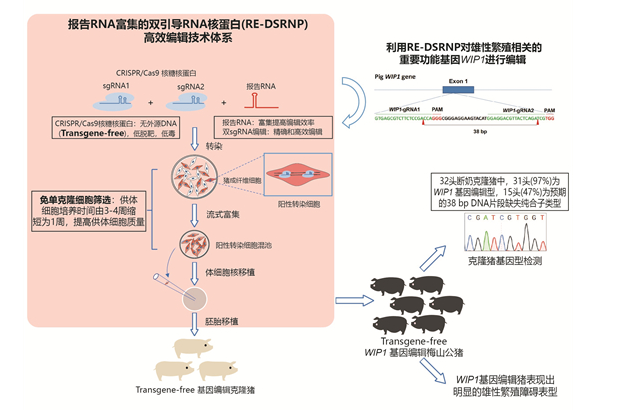
近日,中国农业科学院北京畜牧兽医研究所动物基因工程与种质创新科技创新团队联合深圳农业基因组研究所动物基因组研究中心,成功建立了一种名为报告RNA富集的双引导RNA核 蛋白(RE-DSRNP)的高效编辑技术体系,可用于快速制备无外源DNA基因编辑克隆猪,并利用该体系首次成功获得了 WIP1 基因编辑的雄性繁殖障碍模型猪。相关研究成果发表在《中国科学:生命科学(Science China:Life Sciences)》上。
基因编辑猪在农业和医学等领域具有重要的应用价值,然而,制备基因编辑猪的过程中还存在诸多问题。例如,难以快速获得大量基因型一致的个体,质粒DNA可能随机整合到细胞的基因组,单克隆细胞筛选过程可能降低供体细胞的质量等。
为了完善基因编辑猪的制备过程,研究人员使用双引导RNA,提高了编辑精度和效率;使用核糖核 蛋白编辑系统,成功避免了质粒DNA整合到基因组的风险,实现了低脱靶、低毒、无外源DNA基因编辑;将报告RNA富集系统与双引导RNA核 蛋白(DSRNP)有机结合,建立了RE-DSRNP体系,可使核移植供体细胞的培养时间由3~4周缩短为1周,而且显著降低了供体细胞发生凋亡和染色体异常的比例。为了验证RE-DSRNP在创制基因编辑克隆猪上的应用效果,研究人员以高繁殖力著称的我国地方猪种——梅山猪为材料,利用RE-DSRNP体系靶向编辑 WIP1 基因。结果表明,在获得的32头断奶克隆猪中,有31头为 WIP1 基因编辑型,15头为预期的38bp DNA 片段缺失纯合子类型,所有的克隆猪均未检测到脱靶,且 WIP1 基因编辑猪表现出明显的雄性繁殖障碍表型。
体细胞克隆基因编辑技术是目前动物生物育种和医学模型研发的主流技术。该研究建立的RE-DSRNP体系,可显著降低脱靶和非预期效应,极大提高编辑效率,缩短制备时间,在猪和其他大动物的生物育种以及医学模型研发方面应用前景广阔。此外,种公猪对母猪繁殖力具有决定性作用,在育种体系和商品生产中举足轻重,该研究首次构建了 WIP1 基因编辑猪模型,对于深入研究雄性繁殖机制具有重要意义。
该研究得到国家自然科学基金、中国农科院科技创新工程等项目资助。(通讯员 付松川)(文章来源:中国农业科学院北京畜牧兽医研究所 作者: 王冰源)原文链接:https://doi.org/10.1007/s11427-021-2058-2
3、研究揭示非洲猪瘟病毒拮抗宿主天然免疫应答新机制
近日,中国农业科学院兰州兽医研究所口蹄疫与新发病流行病学创新团队在非洲猪瘟病毒免疫逃逸及致病机制方面研究取得新进展,该研究鉴定了非洲猪瘟病毒新的免疫抑制基因MGF360-9L,证实了MGF360-9L是非洲猪瘟病毒的主要毒力因子之一,系统解释了该基因拮抗宿主天然免疫应答的分子机制,相关研究成果发表在《mBio》。
该研究发现,非洲猪瘟病毒MGF360-9L蛋白能够拮抗JAK-STAT信号通路。进一步研究发现MGF360-9L通过凋亡途径降解STAT1,通过泛素-蛋白酶体途径降解STAT2,从而抑制I型干扰素的信号转导。动物实验结果表明,缺失MGF360-9L基因的重组非洲猪瘟病毒对猪体的致病力显著降低。该研究揭示了非洲猪瘟病毒免疫逃逸的一种新策略,鉴定了一个新的非洲猪瘟病毒的毒力因子,为非洲猪瘟病毒致病机制探索和疫苗的研发提供了新的理论依据。
该研究得到国家重点研发计划等项目的资助。(文章来源:中国农业科学院兰州兽医研究所)
原文链接:https://pubmed.ncbi.nlm.nih.gov/35076286/




发表评论 取消回复